
domingo, 20 de febrero de 2011
miércoles, 16 de febrero de 2011
ALONDRA SARAHI
CAMBIOS QUIMICOS
Balances de masa en las reacciones químicas
Balances de masa en las reacciones químicas
Masa atómica
Los átomos de distintos elementos tienen masas y tamaños diferentes. Los científicos han establecido comparaciones entre las masas y los tamaños de los átomos hoy conocidos.
La escala de masas atómicas asigna masas a los átomos por comparación con la masa del átomo de carbono, al que se le asigna el valor 12. La unidad de masa a escala atómica se denomina unidad de masa atómica y se simboliza con u o uma.
En las tablas periódicas aparece la masa atómica en uma de cada elemento:
Masas moleculares
Una molécula es una agrupación de átomos de la misma o distinta clase. El número de cada clase de átomos viene especificado en la fórmula de la sustancia. Por ejemplo, la fórmula Fe2O3 significa que esta molécula está formada por 2 átomos de hierro y 3 de oxígeno.
La masa molecular se calcula sumando las masas atómicas de todos los átomos que intervienen en la fórmula de la sustancia.
Por tanto, la masa molecular del Fe2O3 será 56·2 + 16·3 = 160 uma.
Cálculos con reacciones químicas
Una reacción ajustada indica las proporciones en las que participan las diversas sustancias. Teniendo en cuenta las masas atómicas o moleculares de las sustancias, podemos establecer qué cantidad (en masa) de cada sustancia interviene en la reacción.
Ejemplo:
2 Fe + O2 → 2 FeO
Consultando una tabla periódica podemos ver que la masa atómica del Fe es 56 uma y la masa molecular del O2 es 32 uma, mientras que la masa del FeO es 56 + 16 = 72 uma. Al observar la reacción ajustada, vemos que la relación de masas que intervienen en la reacción es:
2 · masa Fe + masa O2 → 2 · masa FeO
Es decir:
2 · 56 + 32 → 2 · 72
La misma relación de masas atómicas o moleculares se cumple tanto en unidades de masa atómica como en gramos o en kilogramos. Por tanto, se puede afirmar que 112 g de hierro reaccionan con 32 g de oxígeno atmosférico para producir 144 g de FeO.
Procedimiento de cálculo con reacciones químicas
1.- Ajusta la reacción química.
2.- Determina las masas atómicas o moleculares de las sustancias que intervienen.
3.- Multiplica dichas masas por los correspondientes números enteros que has escrito antes para ajustar la reacción.
4.- Los valores obtenidos, expresados en cualquier unidad de masa, indican las cantidades de reactivo y de producto que intervienen en la reacción.
En general, cuando se forma una sustancia estable (que perdura en el tiempo) a partir de sus elementos, se libera energía, normalmente en forma de energía térmica. Por el contrario, para destruir una sustancia estable, se necesitará aportar energía. Según el balance energético, las reacciones se clasifican en:
Reacción endotérmica: Es aquélla que necesita un aporte de energía para producirse.
Ejemplo: Descomposición del clorato potásico para obtener cloruro potásico y oxígeno.
Reacción exotérmica: Es aquélla que libera energía térmica mientras se produce.
Ejemplo: Combustión del butano para obtener energía térmica para calentar agua.
martes, 15 de febrero de 2011
Ernesto Josue Vazquez Aquino
Las reacciones quimicas no son todas complejas sino solo basta con quemaruna hoja de papel
TAREA ATRASADA DE ALEXIS CASILLAS BERUMEN NUM 5
Las Reacciones Quimicas
Las reacciones químicas son procesos en los que una o más sustancias se transforman en otra u otras con propiedades diferentes. Para que pueda existir una reacción química deben haber sustancias que reaccionan y sustancias que se forman. Se denominará reaccionante o reactivo a la sustancia química que reacciona. A las sustancias que se generan debido a una reacción química se les denomina sustancia resultante o producto químico. Los cambios químicos alteran la estructura interna de las sustancias reaccionantes.
Generalmente, se puede decir que ha ocurrido una reacción si se observa que al interactuar los "supuestos" reaccionantes se da la formación de un precipitado, algún cambio de temperatura, formación de algún gas, cambio de olor o cambio de color durante la reacción.
A fin de expresar matemática una reacción química se hace necesario utilizar una expresión en la cual se señalan los reactivos y los productos. Esta expresión recibe el nombre de ecuación química.
Existen cuatro tipos de reacciones:
a)Combinación
b)Descomposición
c)Desplazamiento
d)Doble combinación
b)Descomposición
c)Desplazamiento
d)Doble combinación
Las reacciones también pueden ser clasificadas en a)Reacción química homogéneas y b)Reacción química heterogénea.
Son mezclas homogéneas.
Al disolver una sustancia, el volumen final es diferente a la suma de los volúmenes del disolvente y el soluto.
La cantidad de soluto y la cantidad de disolvente se encuentran en proporciones que varían entre ciertos límites. Normalmente el disolvente se encuentra en mayor proporción que el soluto, aunque no siempre es así. La proporción en que tengamos el soluto en el seno del disolvente depende del tipo de interacción que se produzca entre ellos. Esta interacción está relacionada con la solubilidad del soluto en el disolvente.
Las propiedades físicas de la solución son diferentes a las del solvente puro: la adición de un soluto a un solvente aumenta su punto de ebullición y disminuye su punto de congelación; la adición de un soluto a un solvente disminuye la presión de vapor de éste.
Clasificación de las disoluciones
Por su estado de agregación
Sólidas
- Sólido en Sólido: Cuando tanto el soluto como el solvente se encuentran en estado sólido. Un ejemplo claro de éste tipo de disoluciones son las aleaciones, como el Zinc en el Estaño.
- Gas en Sólido: Como su definición lo dice, es la mezcla de un gas en un sólido. Un ejemplo puede ser el Hidrógeno (g) en el Paladio(s).
- Líquido en Sólido: Cuando una sustancia líquida se disuelve junto con un sólido. Las Amalgamas se hacen con Mercurio(l) mezclado con Plata(s).
Líquidas
- Sólidos en Líquidos: Este tipo de disoluciones es de las más utilizadas, pues se disuelven por lo general pequeñas cantidades de sustancias sólidas (solutos) en grandes cantidades líquidas (solventes). Ejemplos claros de este tipo son la mezcla del Agua con el Azúcar, también cuando se prepara un Té, o al agregar Sal a la hora de cocinar.
- Gases en Líquidos: Por ejemplo, Oxígeno en Agua.
- Líquidos en Líquidos: Ésta es otra de las disoluciones más utilizadas. Por ejemplo, diferentes mezclas de Alcohol en Agua (cambia la densidad final); un método para volverlas a separar es por destilacióneditar Gaseosas
- Sólidos en Gases: Existen infinidad de disoluciones de este tipo, pues las podemos encontrar en la contaminación al estudiar los componentes del humo por ejemplo, se encontrará que hay varios minerales disueltos en gases.
- Gases en Gases: De igual manera, existe una gran variedad de disoluciones de gases con gases en la atmósfera, como el Oxígeno en Nitrógeno.
- Líquidos en Gases: Este tipo de disoluciones se encuentran en las nieblas
Soluto
Se llama soluto a la sustancia minoritaria (aunque existen excepciones) en una disolución, esta sustancia se encuentra disuelta en un determinado disolvente.
En lenguaje común también se le conoce como la sustancia que se disuelve, por lo que se puede encontrar en un estado de agregación diferente al comienzo del proceso de disolución.Lo más habitual es que se trata de un sólido en un disolvente líquido, lo que origina una solución líquida. Una de las características más significativas de una disolución suele ser su concentración de soluto, o sea una medida de la cantidad de soluto contenida en ella.
Otra característica a considerar sería la facilidad o solubilidad que pueda presentar en el disolvente. La solubilidad de un compuesto químico depende en gran medida de su estructura molecular. En general, los compuestos iónicos y moleculares polares son solubles en disolventes polares como el agua o el etanol; y los compuestos moleculares apolares en disolventes apolares como el hexano, el éter o el tetracloruro de carbono.
Disolvente
Un disolvente o solvente es una sustancia que permite la dispersión de otra en su seno. Es el medio dispersante de la disolución. Normalmente, el disolvente establece el estado físico de la disolución, en conclusión es la que tiene la mayor cantidad
Un disolvente o solvente es una sustancia que permite la dispersión de otra en su seno. Es el medio dispersante de la disolución. Normalmente, el disolvente establece el estado físico de la disolución, por lo que se dice que el disolvente es el componente de una disolución que está en el mismo estado físico que la misma. Usualmente, también es el componente que se encuentra en mayor proporción.Los disolventes forman parte de múltiples aplicaciones: adhesivos, componentes en las pinturas, productos farmaceúticos, para la elaboración de materiales sintéticos, etc.
Las moléculas de disolvente ejercen su acción al interaccionar con las de soluto y rodearlas. Se conoce como solvatación. Solutos polares serán disueltos por disolventes polares al establecerse interacciones electrostáticas entre los dipolos. Los solutos apolares disuelven las sustancias apolares por interacciones entre dipolos inducidos.
El agua es habitualmente denominada el disolvente universal por la gran cantidad de substancias sobre las que puede actuar como disolvente
Clasificación de los disolventes
- Disolventes polares: Son sustancias en cuyas moléculas la distribución de la nube electrónica es asimétrica; por lo tanto, la molécula presenta un polo positivo y otro negativo separados por una cierta distancia. Hay un dipolo permanente. El ejemplo clásico de solvente polar es el agua. Los alcoholes de baja masa molecular también pertenecen a este tipo. Los disolventes polares se pueden subdividir en:
- Disolventes polares próticos: contienen un enlace del O-H o del N-H. Agua (H-O-H), etanol (CH3-CH2-OH) y ácido acético (CH3-C(=O)OH) son disolventes polares próticos.
- Disolventes polares áproticos: son disolventes polares que no tiene enlaces O-H o N-H. La acetona (CH3-C(=O)-CH3) y THF o Tetrahidrofurano son disolventes polares aprótico.
- Disolventes apolares: En general son sustancias de tipo orgánico y en cuyas moléculas la distribución de la nube electrónica es simétrica; por lo tanto, estas sustancias carecen de polo positivo y negativo en sus moléculas. No pueden considerarse dipolos permanentes. Esto no implica que algunos de sus enlaces sean polares. Todo dependerá de la geometría de sus moléculas. Si los momentos dipolares individuales de sus enlaces están compensados, la molécula será, en conjunto, apolar. Algunos disolventes de este tipo son: el dietiléter, cloroformo, benceno, tolueno, xileno, cetonas, hexano, ciclohexano, tetracloruro de carbono es el que disuelve o va a disolver, etc. Un caso especial lo constituyen los líquidos fluorosos, que se comportan como disolventes más apolares que los disolventes orgánicos convencionales
Sarahi Ramirez Vizcaino... Reaccion quimica
Las reacciones químicas son procesos en los que una o más sustancias se transforman en otra u otras con propiedades diferentes. A las sustancias que forman parte de esa reaccion se las llama "reactivos".
cambio quimico _____ hector bautista
LOS CAMBIOS QUÍMICOS
Cambios físicos.-Tienen lugar sin que se altere la estructura y composición de la materia, es decir, las sustancias puras que la componen son las mismas antes y después del cambio.
Cambios químicos.-En un cambio químico o reacción química se altera la estructura y composición de la materia: de unas sustancias iniciales se obtienen otras distintas.
Como reconocer un cambio químico.- Basta observar ciertos indicios como la formación de un precipitado, el cambio de color y sabor o la formación de un gas. Estudio de algunos cambios químicos en la vida diaria.
Cambios en presencia del aire: oxidaciones.
Una oxidación es una reacción de una sustancia con él oxigeno.
Descomposiciones:
Reacciones de síntesis: Obtener moléculas más o menos complejas a partir de otras más sencillas.
Acidez y alcalinidad: reacciones de neutralización.
Ácidos.- La mayoría son solubles en agua como en el caso del vinagre, reaccionan con los metales desprendiendo hidrogeno y formando una sal. Debido a que tienen mucha tendencia a reaccionar con otras sustancias se les considera corrosivos. La llamada lluvia ácida provoca el deterioro de la naturaleza.
Bases.- Son sustancias capaces de neutralizar la acción de los ácidos. Las bases solubles en agua se llaman álcalis.
Existen los compuestos llamados hidróxidos que también son bases.
Como reconocer un ácido o una base: Indicadores.
El ácido acético o el ácido cítrico son considerados ácidos débiles. Pero los usados en laboratorios y procesos industriales como el ácido nítrico y otros son mucho más fuertes. Hay que tener mucho cuidado porque son altamente corrosivos. Para reconocerlos se usan los llamados indicadores que cambian de color según se hallen en presencia de un ácido o una base.
A menudo es más cómodo utilizar una escala de números llamada escala pH. Sus números van del 1 al 14. Las sustancias neutras tienen un pH de 7, los ácidos menores de 7 y las bases mayor. Para conocer el pH se puede utilizar el papel indicador. Reacciones de neutralización. La reacción entre un ácido y una base recibe la neutralización y se forma una sal. Si la base es un hidróxido, los productos de la reacción son una sal y agua.
Conservación de la masa en las reacciones químicas.
La cantidad de materia en una reacción química.- En cualquier reacción química la masa de las sustancias que reaccionan es igual a la masa de los productos de la reacción.
Cambio químico y reordenación de átomos.- En todo cambio químico los átomos son los mismos al finalizar la reacción lo que reagrupados de distinta forma, ya que algunas sustancias se transforman en otras.
Ecuaciones química.- Es la manera de representar una reacción química. En la ecuación se escriben las fórmulas de las sustancias que intervienen en la reacción, a la izquierda las de los reactivos y a la derecha las de los productos.
La relación entre el número de moléculas de cada sustancia viene indicada por medio de unos números que se llaman coeficientes, y que se escriben menos el 1 delante de cada fórmula.
Cambios físicos.-Tienen lugar sin que se altere la estructura y composición de la materia, es decir, las sustancias puras que la componen son las mismas antes y después del cambio.
Cambios químicos.-En un cambio químico o reacción química se altera la estructura y composición de la materia: de unas sustancias iniciales se obtienen otras distintas.
Como reconocer un cambio químico.- Basta observar ciertos indicios como la formación de un precipitado, el cambio de color y sabor o la formación de un gas. Estudio de algunos cambios químicos en la vida diaria.
Cambios en presencia del aire: oxidaciones.
Una oxidación es una reacción de una sustancia con él oxigeno.
Descomposiciones:
Reacciones de síntesis: Obtener moléculas más o menos complejas a partir de otras más sencillas.
Acidez y alcalinidad: reacciones de neutralización.
Ácidos.- La mayoría son solubles en agua como en el caso del vinagre, reaccionan con los metales desprendiendo hidrogeno y formando una sal. Debido a que tienen mucha tendencia a reaccionar con otras sustancias se les considera corrosivos. La llamada lluvia ácida provoca el deterioro de la naturaleza.
Bases.- Son sustancias capaces de neutralizar la acción de los ácidos. Las bases solubles en agua se llaman álcalis.
Existen los compuestos llamados hidróxidos que también son bases.
Como reconocer un ácido o una base: Indicadores.
El ácido acético o el ácido cítrico son considerados ácidos débiles. Pero los usados en laboratorios y procesos industriales como el ácido nítrico y otros son mucho más fuertes. Hay que tener mucho cuidado porque son altamente corrosivos. Para reconocerlos se usan los llamados indicadores que cambian de color según se hallen en presencia de un ácido o una base.
A menudo es más cómodo utilizar una escala de números llamada escala pH. Sus números van del 1 al 14. Las sustancias neutras tienen un pH de 7, los ácidos menores de 7 y las bases mayor. Para conocer el pH se puede utilizar el papel indicador. Reacciones de neutralización. La reacción entre un ácido y una base recibe la neutralización y se forma una sal. Si la base es un hidróxido, los productos de la reacción son una sal y agua.
Conservación de la masa en las reacciones químicas.
La cantidad de materia en una reacción química.- En cualquier reacción química la masa de las sustancias que reaccionan es igual a la masa de los productos de la reacción.
Cambio químico y reordenación de átomos.- En todo cambio químico los átomos son los mismos al finalizar la reacción lo que reagrupados de distinta forma, ya que algunas sustancias se transforman en otras.
Ecuaciones química.- Es la manera de representar una reacción química. En la ecuación se escriben las fórmulas de las sustancias que intervienen en la reacción, a la izquierda las de los reactivos y a la derecha las de los productos.
La relación entre el número de moléculas de cada sustancia viene indicada por medio de unos números que se llaman coeficientes, y que se escriben menos el 1 delante de cada fórmula.
Reacciones Quimicas
Jose Salvador
Aqui les dejo algunos ejemplos de reacciones quimicas para que las analicen...
REACCION QUIMICA JOSE LUISARREOLA PADILLA
REACCION QUIMICA POR ALEXIS CASILLAS BERUMEN ALIAS EL TAMAGOCHI
LO CUAL DEMUESTRA QUE EL ALKASELTZER OSEA EN QUIMICA PARA EL PROFE NaHCO3 + HCit —-> NaCit + CO2 + H2O QUE ES LO QUE HACE QUE AL HACER CONTACTO CON EL AGUA SE AGA ESPUMA
Juan Manuel Ramirez




Kimberly Esparza


luz elena

-Carlos Alejandro Rico-

Sarahi Ramirez Vizcaino
La Reaccion quimica: combustión
Paola Villalaz Meza
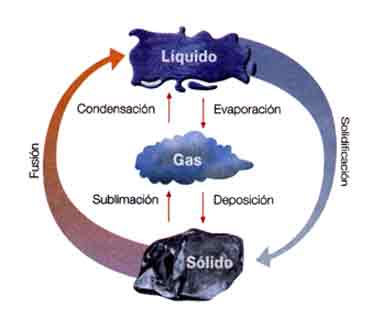

Fatima Daniela Navarro Rodriguez
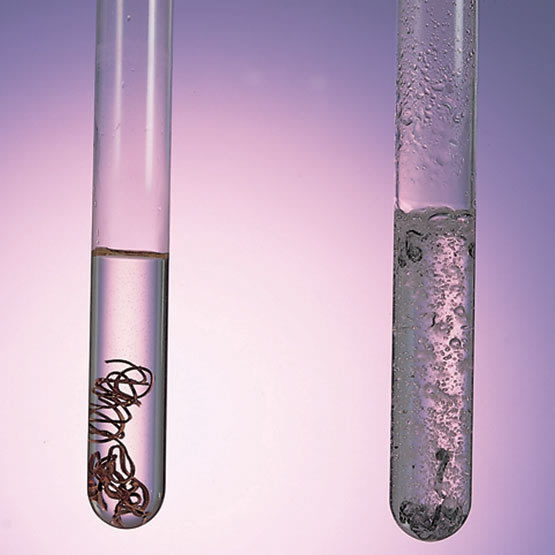
DIANA LAURA
CAMBIO QUIMICO
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
A la representación simbólica de las reacciones se les llama ecuaciones químicas.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química. Estas cantidades constantes, las magnitudes conservadas, incluyen el número de cada tipo de átomo presente, la carga eléctrica y la masa total.
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
A la representación simbólica de las reacciones se les llama ecuaciones químicas.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química. Estas cantidades constantes, las magnitudes conservadas, incluyen el número de cada tipo de átomo presente, la carga eléctrica y la masa total.
lunes, 14 de febrero de 2011
alondra sarahi
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
A la representación simbólica de las reacciones se les llama ecuaciones químicas.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química. Estas cantidades constantes, las magnitudes conservadas, incluyen el número de cada tipo de átomo presente, la carga eléctrica y la masa total.
Jose Salvador:
Una reacción química es un proceso por el cual una o más sustancias, llamadas reactivos, se transforman en otra u otras sustancias con propiedades diferentes, llamadas productos.
En una reacción química, los enlaces entre los átomos que forman los reactivos se rompen. Entonces, los átomos se reorganizan de otro modo, formando nuevos enlaces y dando lugar a una o más sustancias diferentes a las iniciales. La materia puede sufrir cambios mediante diversos procesos. No obstante, todos esos cambios se pueden agrupar en dos tipos: cambios físicos y cambios químicos.
Carlos Rico:
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos.
Lucía Cruz:
Una reacción química es un fenómeno químico en el cual se combinan determinadas sustancias para formar otras o al revés, a partir de determinada sustancia se obtienen otras diferentes.
Kimberly Alejandra Esparza:
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactivos), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos.
Juan Manuel Ramirez:
es el proceso a partir del cual unas sustancias, a las que se llaman reactivos, se transforman en otras llamadas productos. Lo que ocurre en estas reacciones es que las sustancias de partida reorganizan sus átomos.
Elizabeth Esparza:
Jose Salvador:
Una reacción química es un proceso por el cual una o más sustancias, llamadas reactivos, se transforman en otra u otras sustancias con propiedades diferentes, llamadas productos.
En una reacción química, los enlaces entre los átomos que forman los reactivos se rompen. Entonces, los átomos se reorganizan de otro modo, formando nuevos enlaces y dando lugar a una o más sustancias diferentes a las iniciales. La materia puede sufrir cambios mediante diversos procesos. No obstante, todos esos cambios se pueden agrupar en dos tipos: cambios físicos y cambios químicos.
Carlos Rico:
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos.
Lucía Cruz:
Una reacción química es un fenómeno químico en el cual se combinan determinadas sustancias para formar otras o al revés, a partir de determinada sustancia se obtienen otras diferentes.
Kimberly Alejandra Esparza:
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactivos), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos.
Juan Manuel Ramirez:
es el proceso a partir del cual unas sustancias, a las que se llaman reactivos, se transforman en otras llamadas productos. Lo que ocurre en estas reacciones es que las sustancias de partida reorganizan sus átomos.
Elizabeth Esparza:
Es un proceso en el cual una o varias sustancias se transforman en otra (u otras) con propiedades características diferentes.
Ejemplo:
AgNO3 + NaCl ----> AgCl + NaNO3
Nitrato de plata + cloruro de sodio ---> cloruro de plata + nitrato de sodio
Ejemplo:
AgNO3 + NaCl ----> AgCl + NaNO3
Nitrato de plata + cloruro de sodio ---> cloruro de plata + nitrato de sodio
Paola Villalaz Meza:
Una reacción química es un proceso mediante el cual una o más sustancias (elementos o compuestos) denominadas reactivos, sufren una transformación para dar lugar a sustancias diferentes denominadas productos.
José Adrian:
José Adrian:
Una reacción química es el proceso por el cual unas sustancias se transforman en otras .
EJEMPLO: El H2 y el O2 reaccionan para formar un nuevo compuesto H2O.
las sustancias iniciales se llaman reactivos o reactantes y las que resultan se llaman productos.
Ernesto Josue:
Una reacción química es un fenómeno químico en el cual unas sustancias se transforman en otras,, los compuestos que inetractuan se llaman reactivos...
Ernesto Josue:
Una reacción química es un fenómeno químico en el cual unas sustancias se transforman en otras,, los compuestos que inetractuan se llaman reactivos...
luz elena
Cambios físicos.-Tienen lugar sin que se altere la estructura y composición de la materia, es decir, las sustancias puras que la componen son las mismas antes y después del cambio.
Cambios químicos.-En un cambio químico o reacción química se altera la estructura y composición de la materia: de unas sustancias iniciales se obtienen otras distintas.
Como reconocer un cambio químico.- Basta observar ciertos indicios como la formación de un precipitado, el cambio de color y sabor o la formación de un gas. Estudio de algunos cambios químicos en la vida diaria.
Cambios en presencia del aire: oxidaciones.
Una oxidación es una reacción de una sustancia con él oxigeno.
Descomposiciones:
Reacciones de síntesis: Obtener moléculas más o menos complejas a partir de otras más sencillas.
Acidez y alcalinidad: reacciones de neutralización.
Ácidos.- La mayoría son solubles en agua como en el caso del vinagre, reaccionan con los metales desprendiendo hidrogeno y formando una sal. Debido a que tienen mucha tendencia a reaccionar con otras sustancias se les considera corrosivos. La llamada lluvia ácida provoca el deterioro de la naturaleza.
Bases.- Son sustancias capaces de neutralizar la acción de los ácidos. Las bases solubles en agua se llaman álcalis.
Existen los compuestos llamados hidróxidos que también son bases.
Como reconocer un ácido o una base: Indicadores.
El ácido acético o el ácido cítrico son considerados ácidos débiles. Pero los usados en laboratorios y procesos industriales como el ácido nítrico y otros son mucho más fuertes. Hay que tener mucho cuidado porque son altamente corrosivos. Para reconocerlos se usan los llamados indicadores que cambian de color según se hallen en presencia de un ácido o una base.
Alondra estafania
La catálisis es el proceso por el cual se aumenta o disminuye la velocidad de una reacción química. los catalizadores pueden actuar de dos maneras , la primera formando un compuesto intermedio y la segunda, absorción.
Por ejemplo, los que reducen la velocidad de la reacción son denominados “catalizadores negativos” o inhibidores . A su vez, las sustancias que aumentan la actividad de los catalizadores son denominados catalizadores positivos o promotores, y las que los desactivan son denominados venenos catalíticos.
La “producción” de los productos químicos industriales más importantes implica a la catálisis. Por ejemplo, en la reducción del etino a eteno, el catalizador paladio (Pd) es "envenenado" parcialmente con acetato de plomo (II) (Pb(CH3COO)2). Sin la desactivación del catalizador, el eteno producido se reducirá posteriormente a etano.[1] [2]
Por ejemplo, los que reducen la velocidad de la reacción son denominados “catalizadores negativos” o inhibidores . A su vez, las sustancias que aumentan la actividad de los catalizadores son denominados catalizadores positivos o promotores, y las que los desactivan son denominados venenos catalíticos.
La “producción” de los productos químicos industriales más importantes implica a la catálisis. Por ejemplo, en la reducción del etino a eteno, el catalizador paladio (Pd) es "envenenado" parcialmente con acetato de plomo (II) (Pb(CH3COO)2). Sin la desactivación del catalizador, el eteno producido se reducirá posteriormente a etano.[1] [2]
alondra estefania
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
A la representación simbólica de las reacciones se les llama ecuaciones químicas.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química. Estas cantidades constantes, las magnitudes conservadas, incluyen el número de cada tipo de átomo presente, la carga eléctrica y la masa total.
A la representación simbólica de las reacciones se les llama ecuaciones químicas.
Los productos obtenidos a partir de ciertos tipos de reactivos dependen de las condiciones bajo las que se da la reacción química. No obstante, tras un estudio cuidadoso se comprueba que, aunque los productos pueden variar según cambien las condiciones, determinadas cantidades permanecen constantes en cualquier reacción química. Estas cantidades constantes, las magnitudes conservadas, incluyen el número de cada tipo de átomo presente, la carga eléctrica y la masa total.
LOS CAMBIOS QUÍMICOS
Cambios físicos.-Tienen lugar sin que se altere la estructura y composición de la materia, es decir, las sustancias puras que la componen son las mismas antes y después del cambio.
Cambios químicos.-En un cambio químico o reacción química se altera la estructura y composición de la materia: de unas sustancias iniciales se obtienen otras distintas.
Como reconocer un cambio químico.- Basta observar ciertos indicios como la formación de un precipitado, el cambio de color y sabor o la formación de un gas. Estudio de algunos cambios químicos en la vida diaria.
Cambios en presencia del aire: oxidaciones.
Una oxidación es una reacción de una sustancia con él oxigeno.
Descomposiciones:
Reacciones de síntesis: Obtener moléculas más o menos complejas a partir de otras más sencillas.
Acidez y alcalinidad: reacciones de neutralización.
Ácidos.- La mayoría son solubles en agua como en el caso del vinagre, reaccionan con los metales desprendiendo hidrogeno y formando una sal. Debido a que tienen mucha tendencia a reaccionar con otras sustancias se les considera corrosivos. La llamada lluvia ácida provoca el deterioro de la naturaleza.
Bases.- Son sustancias capaces de neutralizar la acción de los ácidos. Las bases solubles en agua se llaman álcalis.
Existen los compuestos llamados hidróxidos que también son bases.
Como reconocer un ácido o una base: Indicadores.
El ácido acético o el ácido cítrico son considerados ácidos débiles. Pero los usados en laboratorios y procesos industriales como el ácido nítrico y otros son mucho más fuertes. Hay que tener mucho cuidado porque son altamente corrosivos. Para reconocerlos se usan los llamados indicadores que cambian de color según se hallen en presencia de un ácido o una base.
A menudo es más cómodo utilizar una escala de números llamada escala pH. Sus números van del 1 al 14. Las sustancias neutras tienen un pH de 7, los ácidos menores de 7 y las bases mayor. Para conocer el pH se puede utilizar el papel indicador. Reacciones de neutralización. La reacción entre un ácido y una base recibe la neutralización y se forma una sal. Si la base es un hidróxido, los productos de la reacción son una sal y agua.
Conservación de la masa en las reacciones químicas.
La cantidad de materia en una reacción química.- En cualquier reacción química la masa de las sustancias que reaccionan es igual a la masa de los productos de la reacción.
Cambio químico y reordenación de átomos.- En todo cambio químico los átomos son los mismos al finalizar la reacción lo que reagrupados de distinta forma, ya que algunas sustancias se transforman en otras.
Ecuaciones química.- Es la manera de representar una reacción química. En la ecuación se escriben las fórmulas de las sustancias que intervienen en la reacción, a la izquierda las de los reactivos y a la derecha las de los productos.
La relación entre el número de moléculas de cada sustancia viene indicada por medio de unos números que se llaman coeficientes, y que se escriben menos el 1 delante de cada fórmula.
Fatima Daniela Navarro Rodriguez
jose luis
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
Una reacción química o cambio químico es todo proceso químico en el cual dos o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden ser elementos o compuestos. Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro.
Suscribirse a:
Comentarios (Atom)








 La reaccion quimica
La reaccion quimica






